대표적 인공지능(AI) 의료기기 업체인 뷰노(338220)가 미국 식품의약국(FDA) 승인에 자신감을 드러냈다. 뷰노메드 딥카스가 먼저 허가를 받을 것으로 예상된다. 허가 시기는 하반기 정도로 관측된다.
5일 바이오헬스케어업계에 따르면 뷰노는 최근 딥카스를 미국 2등급 의료기기(FDA 510K)로 승인받는 전략으로 심사를 추진하고 있다. FDA 510K 인허가 제도는 신청 이후 최종 승인까지 짧게는 7주, 길게는 6개월 소요되는 것으로 알려졌다. 추가적인 권고사항이 있을 경우에는 최대 9개월까지도 걸리지만 뷰노의 경우 미국 혁신의료기기로 지정을 받아 빠른 심사가 가능할 것으로 예상된다. 늦어도 하반기에는 미국 시장을 노릴 수 있다는 의미다.
딥카스, 미국 3조원 대 심정지 예측 시장 잡는다
국내에서 ‘캐시카우’로 성장 중인 뷰노메드 딥카스는 혈압과 맥박, 호흡수, 체온 등 입원 환자의 활력 징후를 분석해 24시간 내 심정지 발생 위험도를 알려주는 제품이다.
뷰노에 따르면 미국 시장에 AI를 적용한 심정지 예측 의료기기는 아직 없다. 미국 시장에서 FDA 승인만 받으면 독보적인 매출 확보가 가능한 상황인 것이다.
|
뷰노가 하반기 FDA 승인을 받으면 매출 상승세는 더 가파를 것으로 예상된다. 뷰노에 따르면 미국 일반병동 심정지 예측 시장 규모는 약 3조원 정도로 추정된다. 점유율 10%만 가져와도 3000억원 정도의 매출을 올릴 수 있는 상황이다.
뷰노 관계자는 “해당 시장 추정치는 국내 연간 시장규모(상급종합병원 + 종합병원)를 기준으로 해외 시장 규모를 추정했다”며 “해외 지역별 시장규모는 기존 글로벌 의료기기가 적용하는 시장계수를 사용했는데 국내와 미국 시장의 규모 차가 상당한 것으로 나왔다”고 설명했다.
페라헬스에 없는 AI 적용한 뷰노...대항마 가능하나
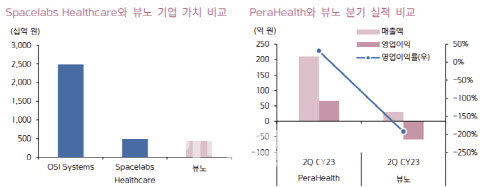
페라헬스 제품은 ‘Rothman Index’라는 지표는 26개의 활력 징후 기반으로 수치화해 응급 상황을 예측, 중환자 분류 등을 돕고 환자 악화 위험 지수 예측 지표를 보여주는 시스템이다. 해당 제품은 기존 솔루션인 ‘MEWS’ 에 비해 정확성이 약 11%p 더 높고, 오경보는 -53% 줄이는 결과를 보여줬다. 이를 기반으로 미국 FDA 인증을 받았고 작년 상반기 미국 상장자 ‘OSI시스템’의 헬스케어 브랜드인 스페이스랩(Spacelabs Healthcare)에 인수됐다.
|
페라헬스의 매출을 보면 뷰노의 미국 시장 진출시 매출을 가늠해 볼 수 있다. 페라헬스의 작년 2분기 매출은 약 220억원, 영업이익 66억원으로 영업이익률 31.3%로 추정된다. 연간 매출 추정치는 약 1000억원이다.
업계 관계자는 “비슷한 제품의 매출 구도를 보면 뷰노 딥카스가 올해 미국 진출 후 달성할 단기 실적 목표를 생각해 볼 수 있다”고 설명했다.







![[포토]크리스마스엔 스케이트](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122500245t.jpg)
![[포토]37번째 거리 성탄예배 열려 방한복·도시락으로 사랑 나눔](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122500231t.jpg)
![[포토]조국혁신당 공수처 앞에서 기자회견](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122500219t.jpg)
![[포토]우리 이웃을 위한 크리스마스 선물](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122500173t.jpg)
![[포토]메리크리스마스](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400797t.jpg)
![[포토]즐거운 눈썰매](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400779t.jpg)
![[포토]취약계층 금융 부담 완화, '인사말하는 이재연 원장'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400633t.jpg)
![[포토]국민의힘 의원총회, '모두발언하는 권성동 원내대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400506t.jpg)
![[포토]윤석열 대통령 탄핵심판 첫 변론 준비기일 27일 예정대로 진행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400433t.jpg)
![[포토]'더불어민주당 원내대책회의'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122400387t.jpg)