[이데일리 김새미 기자] 전날(2일) 국내 제약·바이오 투자 시장에는 큐라티스(348080)가 비만 테마주로 엮이면서 주가가 급등하며 주목 받았다. 이날 압타바이오(293780)와 카이노스메드(284620) 주가의 희비를 가른 것은 기술이전에 대한 기대감이었다. 압타바이오는 기술이전에 대한 기대감이 지속되며 주가가 올랐으나, 카이노스메드는 파킨슨병 치료제 ‘KM-819’의 미국 임상 2상 중간결과 발표에도 기술이전 기대감이 하락하며 주가가 급락했다.
‘비만 테마주’ 큐라티스, 펩진과 협업 강화 가능성에 급등?
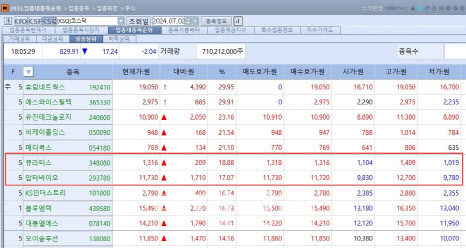
2일 KG제로인 엠피닥터(MP DOCTOR)에 따르면 이날 큐라티스의 주가는 1316원으로 전일 대비 209원(18.88%) 올랐다. 특히 큐라티스의 주가는 이날 오후 12시 46분을 기점으로 급등하기 시작했다. 이날 큐라티스와 관련한 특별한 공시나 뉴스는 없었지만 비만치료제 관련 테마주로 엮이면서 주가가 강세를 보인 것으로 분석된다.
|
펩진이 임상 착수와 글로벌 시장 진출을 위해 상장 제약사와 공동 연구개발 계약을 앞둔 상태인 것으로 알려지면서 이전에 MOU를 체결한 큐라티스에 투자자들의 관심이 쏠린 것으로 추정된다. 펩진 측은 “한 상장 제약사와 공동 연구개발 계약을 곧 마무리할 예정”이며 “해당 제약사는 지분 투자를 통해 전략적 파트너(SI)로 참여하는 것도 계획 중”이라고 언급했다.
단 펩진과 공동 연구개발 계약을 체결할 상장 제약사가 큐라티스인지는 확실치 않다. 큐라티스는 백신 개발 플랫폼 기술을 바탕으로 신약을 개발 중인 회사이기 때문에 비만 치료제와는 거리가 멀다는 지적도 나온다.
업계 관계자는 “큐라티스는 백신을 주로 개발하는 신약개발사로 알고 있다”면서 “비만치료제는 결이 많이 다르고 펩진과 협업하는 부분이 재조합 펩타이드 의약품으로 포괄적이기 때문에 실제로 비만치료제 관련해 추가 협업을 할지는 지켜봐야 할 것”이라고 말했다.
이날 압타바이오의 주가도 전일 대비 1710원(17.07%) 오른 1만 1730원에 거래를 마쳤다. 압타바이오의 주가는 7거래일 만에 76.7% 올랐다. 글로벌 빅파마와 기술이전 및 공동연구 계약을 체결할 것이라는 기대감에 따른 것으로 분석된다. 최근 압타바이오가 기업설명회(IR)에 적극 나서고 있는 것과도 무관치 않다는 해석도 나온다.
압타바이오는 오는 8~9일 여의도에서 기관투자자를 대상으로 기업설명회(NDR)을 진행할 예정이다. 2021년 이후 압타바이오가 시장에 직접 나서는 건 3년 만에 처음이다. 이처럼 압타바이오가 적극적으로 IR에 나서기 시작한 것은 올 하반기부터 각종 모멘텀이 있다는 자신감에 따른 것이다.
압타바이오 관계자는 “바이오USA 전후로 언론과 증권사 리포트 등을 통해 파이프라인의 구체적인 현황이 공유되고 있다”면서 “이전에는 초기 임상 단계라 IR에 적극적으로 나서기 어려웠지만 이제 임상 2상에 진입했거나 진입 예정인 파이프라인이 늘어나면서 좀 더 적극적으로 IR에 나서게 됐다”고 설명했다.
압타바이오의 파이프라인 중 임상 2상 단계에 있는 신약후보물질로는 ‘APX-115’가 있다. APX-115은 당뇨병성신증 임상 2a상을 종료했으며, 조영제유발급성신손상 임상 2상은 진행 중이다. 이 중 조영제유발급성신손상 임상 2상 중 데이터가 오는 9월 중 발표될 예정이다. 해당 결과에 따라 후기 임상 진입 여부가 결정될 예정이다. 두 가지 적응증 모두 빅파마와 기술이전(L/O)을 논의 중인 것으로 알려져 있다.
이전에 빅파마와 실사까지 갔다가 기술이전에 실패했던 황반변성 치료제 ‘APX-1004F’도 최근 빅파마 3곳과 비밀유지계약(CDA)을 맺고 기술이전을 협의 중이다. 면역항암제 ‘APX-343a’는 현재 글로벌 빅파마와 공동연구를 협의 중이며, 이달 중 결론이 날 전망이다.
오병용 한양증권 연구원은 “최근 NOX 저해제에 대한 글로벌 관심이 매우 커진 것으로 보인다”며 “현재 임상 단계의 NOX 저해제 신약을 보유한 기업은 전 세계에 칼리디타스테라퓨틱스(이하 칼리디타스) 두 기업뿐”이라고 짚었다. 이어 “칼리디타스 피인수 발표 이후 다수의 빅파마들이 압타바이오를 찾아와 기술이전을 논의 중”이라고 덧붙였다.
반면 카이노스메드의 주가는 5000원으로 전일 대비 720원(12.59%) 급락했다. 이날 카이노스메드는 파킨슨병 치료제 ‘KM-819’ 미국 임상 2상 중간결과를 발표했다. 일각에선 해당 임상 결과가 공시 없이 언론 보도를 통해서만 공개된 것에 대해 의구심을 제기하기도 했다.
해당 임상 2상은 총 2단계로 약물의 안전성을 평가하는 파트1(Part1)과 약물의 유효성을 평가하는 파트2(Part2)로 나뉜다. 이번에 발표한 중간결과는 파트1에 대한 데이터다.
파트1은 건강한 사람 18명을 대상으로 400mg, 600mg, 800mg의 약물안전성을 확인하는 파트1A와 초기~중기의 파킨슨병 환자들 15명 대상으로 200mg, 300mg의 약물안전성을 확인하는 파트1B로 다시 세분화된다. 이번 중간결과는 파트1B에 따른 결과다.
회사에 따르면 건강한 사람에게 투여된 KM-819는 400mg, 600mg, 800mg까지도 중대한 이상반응은 1건도 없었다. 파킨슨병 환자에게 투여된 용량인 200mg, 300mg에서도 중도탈락 없이 임상을 완료했다. 사망이나 중대한 부작용을 포함한 어떠한 이상반응도 나타나지 않아 환자들에서도 KM-819의 안전성을 확인했다.
카이노스메드는 해당 임상 결과를 바탕으로 기술이전에 박차를 가하겠다는 계획이다. 미국 임상 2상 파트2부터는 대규모 현금 지출이 예상되기 때문이다. 또한 약물에 대한 유효성은 임상 2상 파트2에서 환자 288명을 대상으로 200mg, 300mg의 용량으로 파킨슨병 평가 통합 척도(MDS-UPDRS)와 글로벌 제약사 로슈의 디지털바이오마커를 통해 확인하게 된다.







![[포토] 불길 휩싸인 여객기](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122900445t.jpg)
![[포토]출렁이는 환율 시장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122900259t.jpg)
![[포토]겨울아 반가워](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122900232t.jpg)
![[포토]윤 대통령, '공수처 3차 소환 불응'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122900095t.jpg)
![[포토]한덕수 대통령 권한대행 국무총리 탄핵소추안 투표하는 우원식 국회의장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122700978t.jpg)
![[포토] 달러 상승 이어져...](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122700871t.jpg)
![[포토] 헌법재판소 소심판정](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122700760t.jpg)
![[포토] 정청래 단장과 김이수 전 헌법재판관](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122700742t.jpg)
![[포토] 윤석열 법률대리인 헌재 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122700731t.jpg)
![[포토]내수경기활성화 민당정협의회 열려](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/12/PS24122700609t.jpg)
![[포토]윤이나,후배 양성을 위해 2억원 기부했어요](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24122600088h.jpg)

!["우리 언니 살아있는 거 맞아요?"…통곡으로 가득 찬 무안공항[르포]](https://image.edaily.co.kr/images/vision/files/NP/S/2024/12/PS24122900418b.jpg)

