바이오업계는 그동안 GPCR 모노머(솔로·단량체)를 억제하는 형태의 표적 항암제만 개발됐던 만큼 지피씨알의 표적 항암제가 게임체인저가 될 것으로 기대하고 있다. 지피씨알은 코스닥 상장을 통해 조달되는 자금으로 임상 투자금 등에 사용할 예정이다. 지피씨알은 임상 2상이 마무리되는 2025년쯤 기술 수출을 통한 첫 매출 발생을 목표로 하고 있다.
|
11일 바이오업계에 따르면 지피씨알은 이르면 다음 달 코스닥 상장을 위한 예비심사를 신청할 계획이다. 지피씨알은 지난 6월 코스닥 기술특례 상장을 위한 기술성평가 심사를 통과했다. 기술성 평가는 코스닥 기술 특례 상장을 위한 첫 관문이다.
기술성 평가는 코스닥 기술특례 상장을 준비하는 기업의 핵심 기술과 성장 잠재력을 엄밀히 심사하기 위해 마련됐다. 이를 통과하기 위해 기업들은 한국거래소가 지정한 전문평가기관 2곳에서 각각 A 등급과 BBB 등급 이상을 받아야 한다.
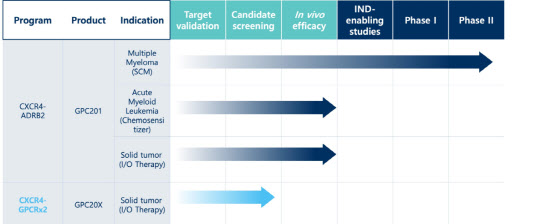
지피씨알은 총 4개의 파이프라인을 보유하고 있다. 이중 가장 앞서 있는 파이프라인은 다발성 골수종(Multiple Myeloma)이 적응증인 ‘GPC201 SCM’이다. GPC201 SCM은 미국 식품의약국(FDA)의 심사를 거쳐 임상 2상을 진행하고 있다. GPC201 SCM은 조혈모세포가동화제로 개발되고 있다. 조혈모세포가동화제란 이식에 사용될 정상적인 조혈모세포를 환자의 말초혈액으로부터 미리 채집하는 과정에서 골수에 모여있는 조혈모세포를 말초혈액으로 이동시키는 의약품을 말한다.
지피씨알 관계자는 “BMS와 사노피, 화이자 등도 GPCR을 타깃으로 한 신약개발에 나서고 있지만 GPCR 모노머를 억제하는 형태”라며 “자사는 GPCR과 ADRB2라는 GPCR 헤테로머를 억제하는 형태로 차이점이 있다”고 설명했다.
그러면서 “모노머가 헤테로머에 비해 분석 실험법 등이 비교적 쉽기 때문”이라며 “자사는 수년간에 걸쳐 GPCR 헤테로머를 개발했고 GPCR과 ADRB2를 억제하는 GPCR 헤테로머 관련 특허를 미국에서 획득했다. GPCR과 다른 물질을 병용하는 경우는 있지만 두 가지 이상의 GPCR들을 병용하는 경우는 전 세계에서 지피씨알밖에 없다”고 말했다.
이어 “GPCR 헤테로머를 억제할 경우 GPCR 모노머를 억제할 때보다 더 많은 조혈모세포들이 말초혈액으로 이동할 수 있다”며 “다발성 골수종 환자들은 최소 300만개 이상의 조혈모세포를 이식받아야 한다. 다수의 조혈모세포를 확보할 수 있다는 것은 곧 치료 효과가 더 좋아진다는 의미”라고 덧붙였다.
임상 2상 2025년 마무리 후 기술 수출 전망
지피씨알은 LG(003550)생명과학 연구원 출신인 신동승 대표를 주축으로 공동 설립자인 허원기 서울대 생명과학부 교수와 피나 카다렐리(Pina Cardarelli) 박사 등 이분야에서 다양한 경험을 가진 인력이 포진해 있다. 특히 최고기술책임자(CTO)인 피나 카다렐리 박사는 면역항암제 옵디보를 개발했다. 피나 카다렐리 박사는 글로벌 빅파마 BMS에서 CXCR4 항체를 개발한 이력도 있다.
업계는 GPC201 SCM의 미국 임상 2상이 2025년 중에 마무리될 것으로 예상한다. 업계는 임상 2상이 마무리되면 지피씨알이 기술 수출로 매출이 발생할 것으로 보고 있다. 지피씨알은 지난해 10월부터 호주 상장 바이오텍 아달타(AdAlta Limited)와 표적 항암제를 공동연구하고 있다.
지피씨알은 2015년부터 4차례에 걸쳐 벤처캐피털 등 20여개의 기관투자자로부터 632억원 규모의 투자금을 유치했다. 지피씨알은 150억~200억원 규모의 상장 전 지분 투자(프리IPO)도 진행하고 있다. 프리IPO는 조만간 마무리될 것으로 전해진다. 기관투자자들이 지피씨알의 기술력을 높이 평가하고 있다는 방증이다. 지피씨알의 기업가치는 1000억원 이상으로 추정된다.
지피씨알 관계자는 “미국 임상 2상 진입을 통해 표적항암제 개발의 첫걸음을 성공적으로 내딛었다고 생각한다”며 “차질없이 계획대로 진행할 수 있도록 최선을 다하겠다”고 말했다.






![[포토] 추위 잊은 송어얼음낚시](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011200345t.jpg)
![[포토]윤석열 대통령 체포영장 2차 집행 초읽기](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011200302t.jpg)
![[포토]설 명절 앞두고 채소값 크게 올라…배추 59%·무 77%↑](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011200259t.jpg)
![[포토]'눈썰매 씽씽'](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011200239t.jpg)
![[포토]올 설날 수산물 할인 '역대 최대'…반값 민생선물세트도 재등장](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011200229t.jpg)
![[포토]민주당 내란특위 외환유치죄 진상조사단, '발언하는 정동영 단장'](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011200165t.jpg)
![[포토]교육부-보건복지부 장관, 의료개혁 관련 브리핑](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011000886t.jpg)
![[포토]제주항공 참사 합동분향소 10일 운영 종료](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011000832t.jpg)
![[포토]박종준 처장, 특수공무집행방해 혐의로 경찰 출석](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25011000511t.jpg)
![[포토] 맘스홀릭베이비페어 전시](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/01/PS25010901108t.jpg)

![[포토]윤혜림-이수정,귀여운 콤비 브이](https://spnimage.edaily.co.kr/images/vision/files/NP/S/2025/01/PS25011200117h.jpg)