|
5일 업계에 따르면, LG화학(051910)은 최근 통풍 치료제 ‘LC350189’의 미국 임상 2상에서 유효성 평가지표를 충족해 신약 개발 가능성을 확인했다. 앞서 JW중외제약(001060)이 지난 3월 통풍 치료제 ‘URC102’의 국내 임상 2b상에서 유효성을 확인한 데 이은 성과다.
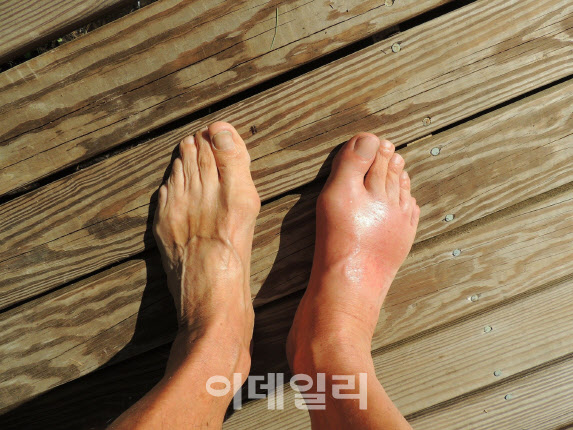
통풍은 단백질 분해 과정에서 나오는 노폐물인 요산이 체내에 과다하게 쌓여 생기는 관절염이다. 크게 요산이 체내에 너무 많이 생성되는 ‘과다생성형’과 요산이 제대로 배출되지 않는 ‘배출저하형’ 질환으로 구분한다. LG화학의 LC350189는 요산 과다 생성을 막아준다. 반면 중외제약의 URC102는 요산 배출을 촉진한다.
임상에서 1차 평가지표인 ‘복용 3개월 시점의 혈청 요산 농도 5mg/㎗(1㎗=0.1ℓ) 미만 달성률’은 LC350189 200mg군이 62%로 나타났다. 반면 위약군 3%, 페북소스타트군이 23%로 나와 LC350189와 큰 차이를 보였다. LC350189 50mg, 100mg 등 저용량군의 달성률도 각각 47%, 45%로 높게 나타났다. 1차 평가지표는 회사가 임상에서 입증하려는 변수로 임상 성패를 가르는 중요 지표다.
JW중외제약도 지난 3월 171명을 대상으로 한 URC102의 국내 임상 2b상에서 유효성을 확인했다. URC102 9㎎, 6㎎, 3㎎ 투여군과 위약 등 총 4개군과 참조군인 페북소스타트 80㎎으로 구분해 12주 동안 약을 투여했다. 1차 평가변수는 ‘약물 투여 후 4주 시점에서의 혈청요산수치 6㎎/㎗ 이하 달성률’로 URC102 9㎎군 89%, URC102 6㎎군 72%, URC102 3㎎군 54%, 위약군 0%로 나타나 모든 URC102 투약군에서 통계적으로 유의했다.
JW중외제약은 국내외 임상 3상을 검토하는 동시에 글로벌 기술수출을 추진 중이다. 앞서 2019년 중국 시장에 대한 URC102의 개발·판매 권리를 중국 심시어제약에 7000만달러(약 836억원) 규모로 이전했다. LG화학 역시 기술수출을 포함해 글로발 신약 개발을 위한 여러 방안을 모색 중이다.









![[포토] 이재경 '핀하이로 쏜다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400197t.jpg)
![[포토] 축시 낭독](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400720t.jpg)
![[포토] 2024 세계한인회장대회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400598t.jpg)
![[포토]유현조,나이스 마무리 퍼트](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400048t.jpg)
![[포토]박도은,핀 공략을 생각한다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300270t.jpg)
![[포토]"예쁜 피부는 역시" 엘렌실라, W페스타 부스 운영](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300485t.jpg)
![[포토]전국 의대 교수, '의평원 무력화 막을 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300350t.jpg)
![[포토]부천국제만화축제 참가한 부천대학교 학생들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300332t.jpg)
![[포토]파란하늘과 가을 꽃](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300310t.jpg)
![[포토]개천절 경축식 만세삼창](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300275t.jpg)
![[포토]임희정,최종일 우승 향한 미소](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100700308t.jpg)



