|
식품의약품안전처는 미국 식품의약국(FDA)이 긴급사용을 승인한 코로나19 혈장 치료와 국내에서 개발하고 있는 혈장(분획)치료제의 차이점에 대해 이 같이 밝혔다.
식약처는 25일 보도자료를 통해 혈장 치료는 소수의 코로나19 완치자로부터 채혈한 회복기혈장을 그대로 환자에게 주입하는 수혈요법이라고 설명했다.
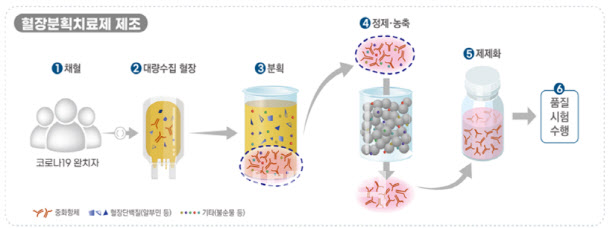
반면 혈장치료제는 한마디로 약(藥)이다. 혈장을 그대로 투여하지 않고 혈장을 활용해 약으로 만든다. 이를 위해 코로나19 완치자의 혈장을 대량 수집 후 분획과정 등을 통해 혈장 속에 포함된 중화항체(면역글로불린)를 정제·농축한다. 이 때문에 혈장치료제에는 고농도의 중화항체가 일정하게 포함돼 있고 혈장치료보다 안전성이 높다고 식약처는 설명했다.
혈장치료제의 경우 현재 GC녹십자(006280)에서 개발하고 있는 ‘GC5131’ 제품이 있다. 이 회사는 지난 20일에 2상 임상시험 계획을 승인받아 임상에 착수했다. 9월 초 첫 환자 등록이 예상된다. 올해 말까지 2상 임상시험을 완료하는 게 목표다.









![[포토] 이재경 '핀하이로 쏜다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400197t.jpg)
![[포토] 축시 낭독](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400720t.jpg)
![[포토] 2024 세계한인회장대회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400598t.jpg)
![[포토]유현조,나이스 마무리 퍼트](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400048t.jpg)
![[포토]박도은,핀 공략을 생각한다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300270t.jpg)
![[포토]"예쁜 피부는 역시" 엘렌실라, W페스타 부스 운영](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300485t.jpg)
![[포토]전국 의대 교수, '의평원 무력화 막을 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300350t.jpg)
![[포토]부천국제만화축제 참가한 부천대학교 학생들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300332t.jpg)
![[포토]파란하늘과 가을 꽃](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300310t.jpg)
![[포토]개천절 경축식 만세삼창](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300275t.jpg)

![[포토]임희정,최종일 우승 향한 미소](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100700308t.jpg)


![영화와는 딴판.. 무도실무관, 현실에선 '삼단봉'도 못쓴다[2024국감]](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100801050b.jpg)