|
셀트리온은 25일(현지시간) 램시마SC를 염증성 장질환 치료제 등으로 사용할 수 있다는 유럽의약품청(EMA) 산하 약물사용자문위원회(CHMP)의 ‘허가 승인 권고’ 의견을 받았다고 29일 밝혔다. CHMP는 과학적 평가 결과를 바탕으로 EMA에 허가 여부 의견을 제시하는 기구다. CHMP의 허가 권고는 사실상 유럽 의약품 승인을 의미하는 것으로 통용된다.
실제 유럽연합 집행위원회 최종 승인은 통상 CHMP의 허가 승인 권고 후 1~3개월 내 이뤄진다. 이에 따라 큰 상황 변경이 없는 한 램시마SC는 조만간 정식 허가를 획득해 기존 류머티즘 관절염 치료에 이어 염증성 장질환 치료제 등으로도 사용될 전망이다. 이번에 승인 권고를 받은 적응증(약 치료 대상)에는 성인을 대상으로 하는 크론병, 궤양성 대장염, 강직성 척추염, 건선성 관절염 및 건선(만성피부질환)이 포함돼 있다.
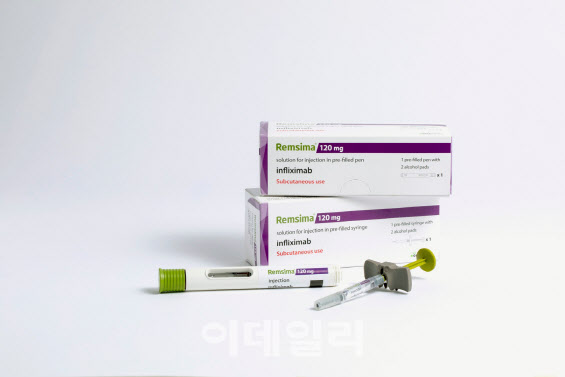
램시마SC는 기존 정맥주사형의 자가면역질환 치료제 램시마를 복부나 허벅지 등에 쉽게 자가주사 할 수 있게 피하주사 제품으로 개선한 제품이다. 정맥주사 제품은 항암제처럼 병원 침대에 누워 4~5시간을 혈관에 맞아야 하기 때문에 복용 편의성이 낮다. 램시마SC는 지난 2월 독일을 시작으로 영국, 네덜란드 등에서 출시돼 있다.
셀트리온 관계자는 “램시마SC의 적응증 추가 허가가 가시화되면서 앞으로 글로벌 자가면역질환 치료 시장에서 입지를 더욱 강화할 것으로 기대한하”며 “램시마SC의 주성분인 인플릭시맙은 염증성 장질환 분야 전문의가 가장 선호하는 성분으로 평가받고 있어 향후 괄목할 만한 시장 점유율이 예상된다”고 말했다.









![[포토] 이재경 '핀하이로 쏜다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400197t.jpg)
![[포토] 축시 낭독](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400720t.jpg)
![[포토] 2024 세계한인회장대회](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400598t.jpg)
![[포토]유현조,나이스 마무리 퍼트](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100400048t.jpg)
![[포토]박도은,핀 공략을 생각한다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300270t.jpg)
![[포토]"예쁜 피부는 역시" 엘렌실라, W페스타 부스 운영](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300485t.jpg)
![[포토]전국 의대 교수, '의평원 무력화 막을 것'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300350t.jpg)
![[포토]부천국제만화축제 참가한 부천대학교 학생들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300332t.jpg)
![[포토]파란하늘과 가을 꽃](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300310t.jpg)
![[포토]개천절 경축식 만세삼창](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100300275t.jpg)

![[포토]임희정,최종일 우승 향한 미소](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24100700308t.jpg)


