뉴스 검색결과 9,286건

- 김강립 신임 식약처장 "백신 유통 개선방안, 올해 안 초안 마련"
- 김강립 신임 식품의약품안전처장[이데일리 노희준 기자] 정부가 올해 안에 백신의 콜드체인(정온배송) 유지 등 백신 유통 전반에 대한 개선책 초안을 마련할 방침이다.김강립 신임 식품의약품안전처장은 독감 백신 ‘상온 노출’ 등 허점이 드러난 백신 유통 체계와 관련, 이르면 올해 안에 콜드체인 유지 방안 등 개선책 초안을 마련하겠다는 의지를 피력했다. 김강립 식약처장은 16일 서울 모처 한식당에서 출입기자단과 취임 후 첫 오찬 간담회를 열고 “가능하면 금년 내까지는 1차적 초안을 마련해 최종적으로 질병관리청과 보건복지부와 논의를 해야 하지 않을까 생각한다”고 말했다. 김 신임 처장은 보건복지부 차관 출신으로 전임 이의경 전 식약처장 후임으로 지난 2일 취임했다. 김 처장은 “질병청 중심으로 정부 TF를 통해 논의를 진행하고 있다”며 “(코로나19) 백신을 공급하고 접종이 이뤄지는 시기 전에는 지금보다 (백신 유통 체계가) 완비돼 있어야 하지 않겠느냐”고 강조했다. 정부는 국가예방접종 사업용 백신이 유통 과정에서 상온에 노출된 사태와 관련, 식약처, 질병청, 복지부 등 관계 부처와 TF를 구성해 유통과정에서의 콜드체인 유지와 백신 배송 및 배분 과정 등에 대한 개선책을 마련하고 있다. 김 처장은 백신 유통 체계 개선 방향에 대해서는 “‘유통(관리)를 다 식약처가 해라’, ‘질병청이 해라’ 그러면 좋지만 둘 다 지방조직이 있지만 (식약처의 경우) 기껏해야 6개 지방청이 있다”며 “막상 (백신) 접종이 이뤄지면 독감 백신만 해도 보건소는 전국에서 200개 넘고, 민간 의료기관도 있어 지방자치단체가 책임을 안 지게 했을 때 문제가 있을 수도 있다”고 설명했다. 그러면서 “이걸(현 체계를) 어떻게 체계적으로 돌아가게 할지 고민하게 하는 게 현실적 대안”이라고 덧붙였다. 현재 독감 접종 대상과 접종 수량 등 국가예방접종 사업 전반은 질병청, 독감 백신 품질 검증은 식약처, 도매업체 선정은 조달청, 도매업체 허가 및 관리감독은 지자체가 맡고 있다.국내보다 먼저 개발될 것으로 예상되는 해외 제약회사의 코로나19 백신 확보 방안에 대해서도 “달리기하듯 1등으로 구매하는 게 목표가 되는 게임은 아니다. 무조건 골라인에 처음 골인하는 이가 우승이 아니고 5등이 우승자가 될 수도 있다”며 “(개발되는 백신마다) 장단점이 있고 효과, 가격, 효과 지속성, 접종 회수, 유통 체계 등 고려할 사항이 많다”고 언급했다.코로나19 백신의 도입 원칙에 대해서도 “신속성과 안전성이라는 조화하기 어려운 두 가치를 동시에 해결해야 한다”며 “안전성을 양보하는 건 있을 수 없지만 안전성을 기반으로 최단 시간에 (백신의 효능을) 검증해야 한다는 숙제가 있다는 것 또한 명확하게 인식하고 있다”고 역설했다. 김 처장은 일러야 내년 연말에야 국내 코로나19 백신 개발이 가능할 것으로 내다봤다. 그는 “(해외의 경우) 3상에 들어가 있는 게 몇 개가 있는데 우리는 2개 제품(제넥신, 국제백신연구소/이노비오)이 이제 (1상에) 들어갔다”며 “정말 여러가지가 잘 겹쳐지면 빨라야 내년 말쯤이라고 볼 수 있어 (해외와) 상당한 시차가 있다”고 했다.행시 출신으로 보건행정을 주로 담당해 의약품 전문성이 떨어지는 것 아니냐는 지적에는 “많은 수의 전문가가 식약처 내에 있다”며 “전문가가 증거를 기반으로 맡은 일을 제대로 할 수 있도록 여건을 만들고 그 결과를 국민이 정책적으로 받아들일 수 있도록 제도화하는 것이 제 일”이라고 설명했다. 김 신임 처장은 연세대 사회학과를 졸업한 행시 35회 출신으로 전통 관료(보건학 박사)다. 그는 “코로나19 백신과 치료제 개발에서 최선을 다하겠다”며 “국민들이 쉽게 이해하고 납득하고 따를 수 없다면 정책의 정당성을 확보할 수 없기에 이해하기 어려운 식약처 정책을 좀더 쉽게 설명할 수 있도록 노력하겠다”고 약속했다.
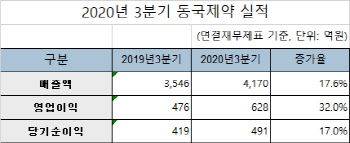
- 동국제약, 3Q 영업익 628억...전년비 32%↑
- [이데일리 노희준 기자] 동국제약(086450)이 3분기 32%의 영업이익 성장세를 보였다. 수출을 비롯해 전 분야가 호조를 보인 덕분이다. 동국제약은 3분기 영업이익이 628억원으로 전년 동기 대비 32% 불어났다고 16일 밝혔다. 같은기간 매출액은 4170억원으로 17.6% 증가했고 당기순이익도 491억원으로 17% 늘었다.회사측은 “일반의약품 사업부, 전문의약품 사업부, 헬스케어 사업부, 해외 사업부, 동국생명과학(자회사) 등 전 사업부에서 고른 성장을 이룬 가운데, 특히 수출과 헬스케어 부문에서 두드러진 성장세를 보였다”고 설명했다. 수출(해외사업부) 부문은 코로나19 펜데믹 상황에서 기존 ‘포폴 주사’뿐만 아니라 항생제 원료의약품인 ‘테이코플라닌’이 기존 수출국가에서 꾸준한 성장세를 보였다. 특히 브라질 수출이 3분기 두각을 드러냈다.또한, 히알루론산(HA) 피부 주름개선 필러 ‘벨라스트’가 아시아 지역에서 수출이 대폭 증가했다.일반의약품(OTC) 부문에서는 먹는 탈모약 ‘판시딜’과 먹는 치질약 ‘치센’, 정맥순환 개선제 ‘센시아’, 여성 갱년기 치료제 훼라민Q 등 성장동력들이 신수요를 창출하며 매출 성장을 견인했다.일반의약품(ETC) 부문에서는 고지혈증 복합제인 ‘로수탄젯’과 ‘피타론에프’ 등 만성질환과 관련된 내과 영역 의약품이 성장을 주도했다.헬스케어 부문에서는 화장품 브랜드 ‘센텔리안24’의 신제품 출시, 헬스앤뷰티(H&B) 제품군 확대, 뷰티 어워드 수상, 중국 진출 등으로 국내외 더마 화장품(기능성 화장품)시장에서 안정적인 성장세를 유지하고 있다.또한, 건강기능식품 브랜드 ‘동영제’, 혈행개선 슬리머 ‘센시안’(혈액순환을 도와주는 압박밴드) 등이 신시장과 신수요를 창출하고 있다. 자회사인 동국생명과학은 주력제품인 ‘파미레이’, ‘유니레이’ 등 조영제가 지속적인 성장을 이루고 있다. 또 이동형CT, 초음파 등 진단장비와 인공지능(AI), 체외진단 등 기타 의료기기 분야로 사업 다각화를 통해 추가적인 성장동력도 확보 중이다.